Pour fin de lecture, les chiffres entre parenthèses réfèrent aux numéros des références annexées au présent document.
Plusieurs personnes souffrent de symptômes gastro-intestinaux (GI). Ballonnements, crampes, constipation ou diarrhée sont souvent des symptômes rapportés lors des rencontres cliniques avec notre clientèle!
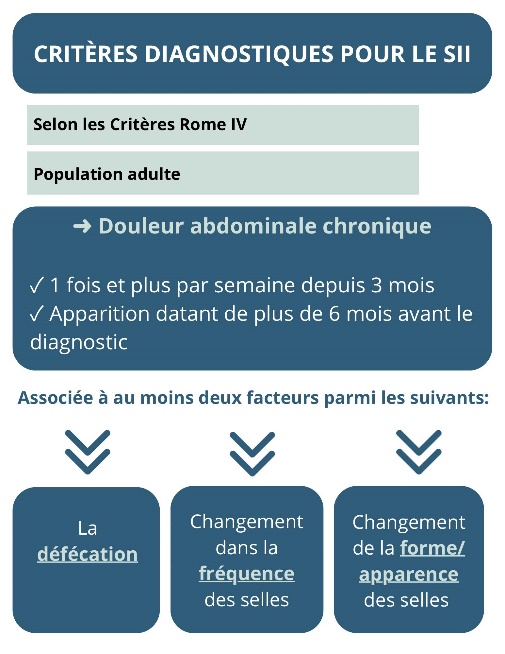
Certaines personnes présentent le diagnostic du syndrome de l’intestin irritable (SII) (auparavant appelé côlon irritable) basé sur différents critères diagnostiques et ce, selon les symptômes décrits et leur fréquence (2). On estime qu’entre 5 et 10% de la population mondiale a un SII (2). Cette condition touche généralement, davantage les femmes et les personnes de moins de 50 ans (8, 15).
On catégorise le SII en 4 groupes (2, 10, 11, 15) :
✔ SII constipation (SII-C)
✔ SII diarrhée (SII-D)
✔ SII mixte : alternance entre diarrhée et constipation (SII-M)
✔ SII non spécifié (SII-U)
Adapté de Jayasinghe et al. (2023) (11)
Vous l’aurez compris, le SII est donc une « maladie d’exclusion » par la présence de symptômes GI sans maladie (ex. maladie cœliaque, maladie de Crohn, colite ulcéreuse) les expliquant.
Le but de l’approche nutritionnelle vise à assurer la gestion des symptômes GI, à identifier les intolérances alimentaires (s’il y a lieu), à combler les besoins nutritionnels et à optimiser la santé microbienne.
Étant donné que les symptômes GI sont souvent liés à la consommation d’aliments, la nutrition est au centre des interventions (1, 3)! À ce sujet, plusieurs organisations dont l’Association américaine de gastroentérologie (American Gastroenterological Association) recommandent une référence en nutrition pour toute personne ayant un SII (1). De plus, la littérature rapporte que les sujets ayant un SII ont généralement des niveaux plus faibles de vitamines B1 et B2, de calcium, de fer et de zinc comparativement aux sujets sans SII (3).
Vous n’êtes donc pas seul(e) dans cette situation! Mais, quelles sont les solutions? Doit-on absolument suivre les principes de l’alimentation faible en FODMAP pour avoir une amélioration des symptômes
Commençons par les trucs de « base »
Étant donné que les symptômes GI sont très individuels, une approche personnalisée est essentielle.
Voici tout de même quelques conseils nutritionnels généraux qui peuvent aider à gérer les symptômes, basés sur le National Institute for Health and Care Excellence (NICE) (1, 4, 15, 17).
| Recommandations | Explications | Applications |
| Réduire l’aérophagie ; | Limite les apports en « air » ingéré pour réduire les ballonnements et gonflements; | Manger lentement (min. 15 minutes par repas); Bien mastiquer les aliments Réduire la consommation de liquides pétillants (ex. eau pétillante, bière); Ne pas parler en mangeant; Ne pas utiliser de paille; Ne pas mâcher de la gomme; |
| Avoir une routine alimentaire; | Permet de répartir les apports dans la journée et favorise l’écoute de la faim et de la satiété; | Manger 3 repas par jour selon un horaire « fixe »; Ajouter des collations au besoin; Ne pas sauter de repas; S’asseoir pour manger; Bien écouter la satiété lors des repas; |
| Réduire les aliments gazogènes; | Limite la « fermentation » à l’intestin pouvant occasionner des gaz; | Limiter les aliments suivants : Famille des choux (brocoli, chou-fleur, chou vert, navet, chou de Bruxelles); Ail et oignon; Légumineuses (pois chiches, haricots); Grande quantité de crudités; |
| Limiter les apports de féculents/sucres (glucides) aux repas; | Consommés en excès lors d’un même repas, les glucides favorisent des gonflements et des ballonnements; | Limiter les apports au ¼ de l’assiette en féculents (pain, riz, pâtes, couscous, pommes de terre, craquelins); Limiter les sucres ajoutés (gâteaux, biscuits, boissons gazeuses); Miser sur des féculents généralement bien tolérés (ex. avoine, quinoa, sarrasin, patate douce); Viser max. 3 fruits par jour, répartis dans la journée; |
| Limiter la consommation d’aliments ayant des édulcorants; | Peuvent provoquer des troubles GI; | Limiter la consommation d’aliments ayant des sucres alcool (ex. sorbitol, mannitol, xylitol) et de l’aspartame comme les produits sans sucre, les bonbons, les gommes et les boissons diètes ; |
| Limiter les apports en gras ajoutés; | Consommés en grande quantité, les gras ralentissent la vidange gastrique; | Réduire la consommation de friture, panure, sauces et viandes grasses; Miser sur des gras généralement bien tolérés, en petites quantités (avocat, noix, graines, huiles); |
| Limiter les aliments généralement irritants; | Peuvent nuire à la digestion globale; | Limiter la caféine, les aliments épicés et l’alcool; |
| Avoir des apports hydriques adéquats; | Aide à la régularité intestinale; | Viser 1,5 à 2L d’eau par jour; S’assurer d’avoir une urine claire dans la journée; Limiter les apports aux repas au maximum, boire entre les repas; |
En bref, le plus grand défi est de trouver les solutions qui fonctionnent pour vous! Chaque cas de SII est unique, d’où la personnification de la démarche! Prenez rendez-vous avec une nutritionniste de notre équipe pour une approche qui tienne compte de votre réalité globale !
Et les fibres?
Les fibres peuvent avoir deux rôles lors du SII : nuire ou aider! En effet, selon vos symptômes et les types de fibres, elles n’ont pas le même impact (10). Les fibres insolubles (ex. blé, son de blé) sont généralement plus fermentescibles et peuvent générer plus de ballonnements, de gaz et des douleurs abdominales (1, 2, 8, 15). De leur côté, les fibres solubles sont généralement mieux tolérées (1, 2). À ce sujet, une méta-analyse de 14 études contrôlées randomisées a rapporté un bienfait significatif des fibres sur les symptômes globaux de SII (4, 10). Lors de sous-analyses, les bienfaits étaient associés au psyllium (fibres plus solubles) et non au blé (fibres insolubles) (4, 10). C’est pour cette raison, qu’en général, les suppléments de fibres recommandés sont le psyllium ou les graines de lin moulues (2).
Le sujet des fibres est très complexe et se doit d’être personnalisé à chaque pathologie et à chaque individu.
Et bien oui, le stress!
On entend souvent que le microbiote est notre 2e cerveau. Pour aller plus loin dans ces concepts voir le blogue Alimentation et santé mentale : optimiser ses fonctions cognitives grâce au contenu de son assiette.
En fait, cette relation est dans les deux sens (bidirectionnelle) surtout lorsqu’il est question de stress (état d’inquiétude ou de tension mentale causé par une situation difficile). Le stress aurait un impact sur les symptômes GI et à l’inverse les symptômes GI pourraient créer un stress (4). On estime que 70 à 90% des patients ayant un SII souffre d’anxiété et de dépression (18). Le stress psychologique a des impacts sur la sensibilité, la motilité, la sécrétion et la perméabilité intestinale (14). Différents mécanismes peuvent expliquer ces impacts dont l’activation immunitaire des muqueuses, des altérations du système nerveux central et le microbiote intestinal altéré (14). La gestion du stress par différentes approches tels les traitements psychologiques incluant la thérapie cognitivo-comportementale et les approches pharmacologiques peut être envisagée (11, 14, 18). La pratique de yoga, l’hypnose, la relaxation, la méditation et les exercices de respiration seraient également des pistes de gestion du stress rapportées dans la littérature (1, 7, 11, 15). Le rire pourrait être également bénéfique (18). Les thérapies par le rire auraient démontré des effets positifs sur la santé physique et mentale, comme des changements sur le système immunitaire, le confort musculaire et les hormones (18). Des études ont démontré que le rire pourrait augmenter les endorphines du cerveau et que 5 minutes de rire pourraient libérer 5 heures de douleur (18).
Bouger, bouger, bouger
Les bienfaits de l’activité physique sont largement documentés et l’intestin ne fait pas exception! En effet, les recommandations du NICE encouragent la pratique d’activité physique (2, 15). En respectant les symptômes GI, l’activité physique peut accélérer le transit GI, améliorer la libération des gaz pour les gens ayant des ballonnements et peut contribuer à augmenter la diversité microbienne (4). De plus, l’activité physique aide à réguler le stress en plus d’améliorer l’humeur et le bien-être (15). Une revue systématique de 14 études contrôlées randomisées a conclu que l’activité physique semble être un traitement efficace pour les patients ayant un SII (4). Des activités douces et de faible intensité sont généralement recommandées comme la marche, le yoga, le cyclisme, la natation et l’aérobie (15).
Bien sûr le microbiote!
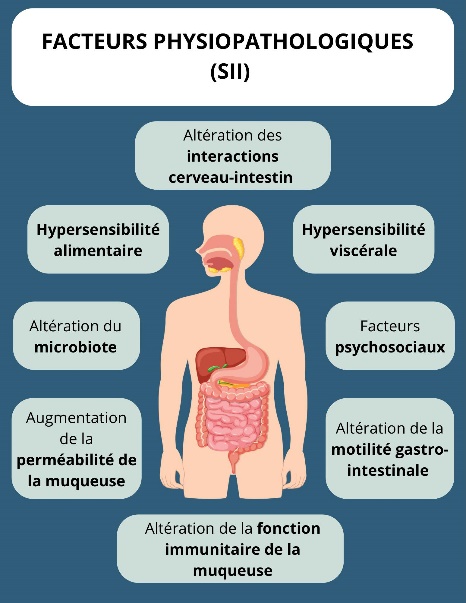
Étant donné que le SII signifie des troubles GI, il est naturel de croire que le microbiote a un rôle à jouer! En effet, dans différentes études observationnelles, la composition des bactéries intestinales diffèrerait entre les sujets ayant un SII et ceux « témoin » (2, 6). Par exemple, une réduction des Lactobacillus et Bifidobactéries a été observée chez les sujets ayant un SII (vs groupe témoin) (6, 8). La littérature rapporte également une diversité bactérienne moindre et une augmentation de la perméabilité intestinale chez cette population (2, 6). De plus, l’intestin des personnes ayant un SII présenterait une densité réduite de cellules endocrines (8). L’expression endocrinienne anormale de l’intestin provoque, en partie, une dysmotilité intestinale (dysfonctionnement des muscles ou des nerfs du système digestif) et une hypersensibilité viscérale (altération du transit et de la perméabilité intestinale), mécanismes impliquant certains symptômes du SII (8).
Les probiotiques et le SII
Les études des bienfaits des probiotiques restent toujours un défi au niveau de la science. En effet, chaque probiotique a une composition différente et notre microbiote personnel est unique. De plus, les différentes études effectuent des protocoles divers (durée, dosage) sur plusieurs populations. En terme scientifique, on parle alors d’une hétérogénéité entre les études, rendant difficile d’en tirer des conclusions claires et précises sur les types de souches et les quantités à viser (6). Différentes études démontrent quand même l’amélioration des symptômes globaux lors de SII par la prise de différentes souches de bactéries avec les probiotiques (vs les groupes témoin) (4, 6). En plus de la restauration de la dysbiose du microbiote intestinal, les probiotiques pourraient moduler la motilité GI, affecter positivement la perméabilité intestinale et réduire l’activation de la muqueuse immunitaire (8). Un Guide clinique existe à ce sujet regroupant différentes études sur les produits disponibles sur le marché avec différentes conditions de santé et leur niveau d’évidence scientifique.
Cliquez ici pour consulter le guide en question.
Pour des conseils plus personnalisés sur les bienfaits possibles d’un probiotique selon vos symptômes, prenez rendez-vous avec l’une de nos nutritionnistes!
Alors les FODMAP sont-ils nécessaires?
Ce concept repose sur les aliments dits « fermentescibles » à l’intestin (13). Ces glucides sont fermentés au côlon, causant des gaz dans le tractus GI bas (2). Pour bien vulgariser le tout : vos bactéries sont « excitées » par la présence de certains sucres (les FODMAP), s’amusent (fermentent) et génèrent des gaz! En réduisant ces types d’aliments, les bactéries réduisent leurs « réactions » associées et améliorent les symptômes! Les FODMAP peuvent également avoir un effet osmotique, menant une augmentation du contenu en eau dans la lumière intestinale, favorisant sa distension menant à des symptômes comme la douleur abdominale, la diarrhée, la flatulence et les ballonnements (2).
L’alimentation faible en FODMAP apporterait dans la grande majorité du temps une amélioration significative des symptômes intestinaux, soit un taux d’efficacité estimé entre 60-75% des cas (12, 16). Cette approche a été largement étudiée dans la littérature scientifique et a démontré ses bienfaits (1). Une méta-analyse de 13 études contrôlées randomisées a évalué les bienfaits sur les symptômes intestinaux de l’alimentation faible en FODMAP comparativement à d’autres approches « traditionnelles » nutritionnelles dont le NICE (5). Selon les analyses, l’approche FODMAP serait supérieure aux autres approches sur l’amélioration des symptômes globaux GI (5).
Comme mentionné, l’alimentation faible en FODMAP n’apporterait pas des bienfaits pour tous, ni de la même façon. Différentes observations ont été faites dans la littérature sur les « répondeurs » vs les « non-répondeurs » aux FODMAP. L’une d’elles réfère à la fonction de la barrière colique et les jonctions serrées…donc le microbiote (16, 17)! Plus d’études sont nécessaires pour confirmer toutes ces observations.
Pour aller plus loin, dans les notions de barrière intestinale, perméabilité et microbiote : allez voir cet article de blogue Perméabilité ou « leaky gut » ce qu’il importe de savoir!
FODMAP
F : Fermentable
O : Oligosaccharides
D : Disaccharides
M : Monosaccharides
And
P : Polyols
Exemples d’aliments riches en FODMAP: melon d’eau, pomme, poire, miel, chou-fleur, lait, ail, oignon, blé, noix de cajou, pois chiches
L’alimentation faible en FODMAP s’effectue en 3 étapes (13).
Étape 1 : Élimination
Pendant 2 à 6 semaines, on cesse les aliments riches en FODMAP. En effet, l’alimentation faible en FODMAP ne doit pas être faite à long terme étant donné que les aliments à limiter sont nombreux.
Cette alimentation peut contribuer à des déficiences en vitamines et minéraux étant donné que les apports alimentaires en vitamines B1, B2 et B9, en calcium, en fer et en magnésium sont réduits lors de son application (3). D’où l’importance d’être encadré par une nutritionniste!
D’ailleurs, la vitamine D a été étudiée dans plusieurs contextes intestinaux (3, 15), voir le Blogue La vitamine D : quoi de neuf? pour plus de détails.
Les FODMAP ont également un effet sur le microbiote par la diminution de la diversité du microbiote et de certaines bactéries bénéfiques, dont les Bifidobacterium (2, 5, 15). Raison de plus de ne pas le faire à long terme!
Étape 2 : Réexposition
À la suite du retrait temporaire des FODMAP, il faut « tester » pour chaque groupe d’aliments, lequel ou lesquels causent les symptômes GI, nommé l’étape 2 (13). Cette étape est essentielle pour ne pas vous limiter inutilement dans vos choix alimentaires! Dans la littérature (et en clinique aussi!), ce sont généralement les groupes d’aliments des fructane (ex. blé, ail, oignon), mannitol (ex. chou-fleur, céleri) et galacto-oligosaccharides (GOS) (ex. pois chiches, boisson de soya) qui créent des symptômes (17).
Étape 3 : Réintroduction
Lors de l’étape 3, on vise à réintroduire les aliments selon les résultats pour chaque groupe d’aliments de l’étape 2 pour évaluer la tolérance (13).
Intolérance au lactose et allergies aux protéines bovines
Le lactose fait partie d’une famille des FODMAP, les disaccharides, étant composé de deux sucres le glucose et le galactose (2, 15). Pour différentes raisons dont génétiques, l’enzyme qui scinde ces deux sucres, lactase, peut être déficient et causer des inconforts digestifs (2, 15). Ainsi, lorsqu’il n’est pas digéré au petit intestin, le lactose peut causer des flatulences, des gonflements, des crampes et des diarrhées (2). En testant le retrait du lactose, par exemple en misant sur du lait et du yogourt sans lactose, vous devriez voir rapidement une amélioration des symptômes digestifs si l’intolérance est présente.
Cela diffère de l’allergie aux protéines laitières, dont le lactosérum et la caséine (2). Ces réactions allergiques peuvent être médiées par les immunoglobulines E ou non (2). Les symptômes peuvent être des lésions cutanées, une détresse respiratoire et des symptômes GI tels qu’une perte de sang rectal et une diarrhée sévère (2).
Gluten vs blé
De son côté, le sucre du blé (fructane) peut être une cause des inconforts intestinaux. Cependant, certaines personnes rapportent avoir des inconforts non seulement au blé, mais aussi au gluten ce qui inclut entre autres le blé, l’orge, l’avoine, le seigle et l’épeautre. En effet, il est possible d’avoir une sensibilité au gluten non cœliaque caractérisée par la présence d’inconforts digestifs lors de la consommation de gluten alors que la maladie de cœliaque et l’allergie au blé ont été exclues lors des investigations médicales (2, 9). Pour le moment, il n’existe pas de test « diagnostic » pour cette intolérance au gluten. Il faut faire des tests alimentaires d’exclusion et de réintroduction en observant les symptômes associés. En outre, la littérature ne démontre pas de bienfaits significatifs de l’alimentation sans gluten lors de SII (10, 15). Bien cibler vos intolérances (blé vs gluten) est essentiel pour limiter les restrictions inutiles.
Vous constatez que le SII est une pathologie complexe et que l’alimentation est au cœur du traitement des symptômes intestinaux associés!
Vos symptômes sont encore présents après l’application de ces conseils généraux? Vous voudriez aller plus loin dans les sujets tels que la constipation et la diarrhée : prenez rendez-vous avec l’une de nos nutritionnistes pour personnaliser votre démarche!
Références :
(1) American Gastroenterological Association. Chey WD, Hashash JG, Manning L, Chang L. AGA Clinical Practice Update on the Role of Diet in Irritable Bowel Syndrome: Expert Review. Gastroenterology. 2022 May;162(6):1737-1745.e5. https://pubmed.ncbi.nlm.nih.gov/35337654/
(2) Algera J, Colomier E, Simrén M. The Dietary Management of Patients with Irritable Bowel Syndrome: A Narrative Review of the Existing and Emerging Evidence. Nutrients. 2019 Sep 9;11(9):2162. https://pubmed.ncbi.nlm.nih.gov/31505870/
(3) Bek S, Teo YN, Tan XH, Fan KHR, Siah KTH. Association between irritable bowel syndrome and micronutrients: A systematic review. J Gastroenterol Hepatol. 2022 Aug;37(8):1485-1497. https://pubmed.ncbi.nlm.nih.gov/35581170/
(4) Black CJ, Ford AC. Best management of irritable bowel syndrome. Frontline Gastroenterol. 2020 May 28;12(4):303-315. https://pubmed.ncbi.nlm.nih.gov/34249316/
(5) Black CJ, Staudacher HM, Ford AC. Efficacy of a low FODMAP diet in irritable bowel syndrome: systematic review and network meta-analysis. Gut. 2022 Jun;71(6):1117-1126. https://pubmed.ncbi.nlm.nih.gov/34376515/
(6) Distrutti E, Monaldi L, Ricci P, Fiorucci S. Gut microbiota role in irritable bowel syndrome: New therapeutic strategies. World J Gastroenterol. 2016 Feb 21;22(7):2219-41. https://pubmed.ncbi.nlm.nih.gov/26900286/
(7) Formation Dietitian Deep Dive, Part 2 : IBS D Management including assessment processes, diet interventions, and non diet interventions, 2023
(8) Galica AN, Galica R, Dumitrașcu DL. Diet, fibers, and probiotics for irritable bowel syndrome. J Med Life. 2022 Feb;15(2):174-179. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8999090/
(9) Guandalini S, Polanco I. Nonceliac gluten sensitivity or wheat intolerance syndrome? J Pediatr. 2015 Apr;166(4):805-11. https://pubmed.ncbi.nlm.nih.gov/25662287/
(10) Jadhav A, Bajaj A, Xiao Y, Markandey M, Ahuja V, Kashyap PC. Role of Diet-Microbiome Interaction in Gastrointestinal Disorders and Strategies to Modulate Them with Microbiome-Targeted Therapies. Annu Rev Nutr. 2023 Aug 21;43:355-383. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10577587/
(11) Jayasinghe M, Damianos JA, Prathiraja O, Oorloff MD, Nagalmulla K GM, Nadella A, Caldera D, Mohtashim A. Irritable Bowel Syndrome: Treating the Gut and Brain/Mind at the Same Time. Cureus. 2023 Aug 13;15(8):e43404. https://pubmed.ncbi.nlm.nih.gov/37706135/
(12) Monash University, Are you suffering from IBS? Page consulté en ligne : https://www.monashfodmap.com/ibs-central/i-have-ibs/
(13) Monash University, Starting the FODMAP diet. Page consultée en ligne : https://www.monashfodmap.com/ibs-central/i-have-ibs/starting-the-low-fodmap-diet/
(14) Qin HY, Cheng CW, Tang XD, Bian ZX. Impact of psychological stress on irritable bowel syndrome. World J Gastroenterol. 2014 Oct 21;20(39):14126-31. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4202343/
(15) Radziszewska M, Smarkusz-Zarzecka J, Ostrowska L. Nutrition, Physical Activity and Supplementation in Irritable Bowel Syndrome. Nutrients. 2023 Aug 21;15(16):3662. https://pubmed.ncbi.nlm.nih.gov/37630852/
(16) Singh P, Grabauskas G, Zhou SY, Gao J, Zhang Y, Owyang C. High FODMAP diet causes barrier loss via lipopolysaccharide-mediated mast cell activation. JCI Insight. 2021 Nov 22;6(22):e146529. https://pubmed.ncbi.nlm.nih.gov/34618688/
(17) Singh P, Tuck C, Gibson PR, Chey WD. The Role of Food in the Treatment of Bowel Disorders: Focus on Irritable Bowel Syndrome and Functional Constipation. Am J Gastroenterol. 2022 Jun 1;117(6):947-957. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9169760/
(18) Tavakoli T, Davoodi N, Jafar Tabatabaee TS, Rostami Z, Mollaei H, Salmani F, Ayati S, Tabrizi S. Comparison of Laughter Yoga and Anti-Anxiety Medication on Anxiety and Gastrointestinal Symptoms of Patients with Irritable Bowel Syndrome. Middle East J Dig Dis. 2019 Oct;11(4):211-217. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6895849/